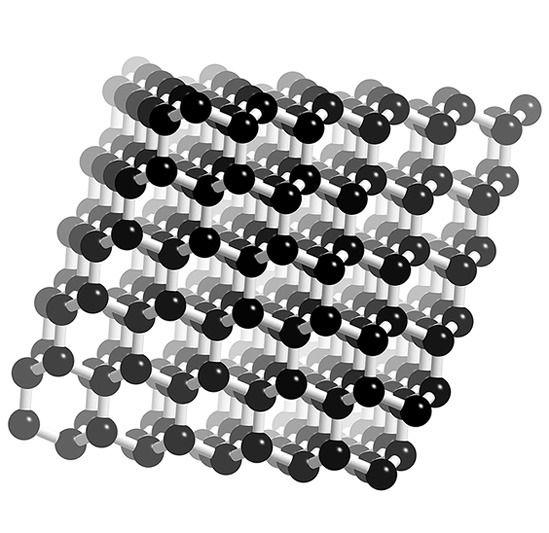
प्रत्येक पदार्थ तीन अवस्थायों में पाया जाता है : (i) ठोस (ii) द्रव (iii) गैस |
पदार्थ की विभिन्न अवस्थायों में अणुओं कीगति भिन्न भिन्न प्रकार की होती है, अंतरा-अणुक दूरी भिन्न-भिन्न होती है तथा अंतरा-अणुक बल भी भिन्न-भिन्न होता है | इसीलिए पदार्थ की विभिन्न अवस्थायों में भौतिक गुण भी भिन्न-भिन्न होते हैं | उदाहरण के लिए, पदार्थ की ठोस अवस्था में उसका एक निश्चित आयतन व निश्चित आकृति होती है, द्रव अवस्था में उसका आयतन को निश्चित होता है लेकिन आकृति कोई निश्चित नहीं होती है तथा गैस अवस्था में न तो आयतन निश्चित होता है न ही आकृति | इन गुणों की व्याख्या अणुगति सिद्धांत द्वारा की जाती है |
ठोस का अणुगति सिद्धांत
ठोस के गुणों की व्याख्या ठोस के अणुगति सिद्धांत द्वारा की जा सकती है, जो निम्न है –
- ठोस के अणु एक नियमित क्रम में सजे होते हैं | प्रत्येक अणु की एक निश्चित अवधि होती है | ये अणु अपनी स्थिति के इधर उधर कम्पनिक गति करते रहते हैं, लेकिन अपना स्थान नहीं छोड़ते हैं | इसीलिए ठोस का आयतन तथा आकृति निश्चित होती है |
- ठोस में अंतरा-अणुक दूरी बहुत कम होती है | सामान्यतः यह अंतरा-अणुक दूरी, द्रव के अपेक्षा कम होती है |
- ठोस में अणुओं के बीच सर्वाधिक आकर्षण बल लगता है | इसी बल के कारण ठोस में अणु अपने स्थान पर बने रहते हैं तथा एक स्थान से दूसरे स्थान तक चलने के लिए स्वतंत्र नहीं होते हैं, बल्कि अपने स्थान पर रहकर ही इधर उधर कम्पनिक गति करते हैं |
- ठोस को गर्म करने पर उसके अणुओं का दोलन आयाम बढ़ जाता है जिससे उनके बीच की औसत दूरी बढ़ जाती है अर्थात ठोस का प्रसार हो जाता है | इसे ठोस का उष्मीय प्रसार कहते हैं |
द्रव का अणुगति सिद्धांत
- द्रव में अणुओं की स्थिति निश्चित नहीं होती हैं, केवल वे द्रव के भीतर ही विभिन्न चालो से विभिन्न दिशाओ में अनियमित गति करते रहते हैं |
- द्रव में अंतरा-अणुक दूरी प्राय ठोस से अधिक होती है, लेकिन गैस की अपेक्षा काफी कम होती है |
- आकर्षण बल, गैस की अपेक्षा बहुत अधिक होता है, लेकिन ठोस की अपेक्षा बहुत कम होता है |
- द्रव को गर्म करने पर उसके अणुओं के बीच की औसत दूरी बढ़ जाती है, जिससे द्रव का उष्मीय प्रसार कहते हैं |
- द्रव को बहुत अधिक गर्म करते रहने पर एक ऐसी अवस्था आती है, जबकि अणुओं की औसत उर्जा इतनी बढ़ जाती है की वे पारस्परिक आकर्षण बल को पार करके द्रव की सतह के बाहर जाने के लिए स्वतंत्र हो जाते हैं | इसे द्रव का वाष्पन कहते हैं |
गैस का अणुगति सिद्धांत
- किसी गैस के सभी अणु समान, सुदृढ़ तथा अति-सूक्ष्म गोलाकार कण होते हैं | इनका आयतन, गैस के आयतन की तुलना में नगण्य होता है |
- गैस के अणुओं की स्थित निश्चित नहीं होती |
- गैस में अंतरा-अणुक दूरी सबसे अधिक होती है |
- गैसों में अणुओं के बीच आकर्षण बल प्रायः नगण्य होता है | इसीलिए अणुओं की गति अनियमित होती है |